地舒单抗在骨质疏松症临床合理用药的中国专家建议
2021-12-30 文章来源:中华骨质疏松和骨矿盐疾病杂志 作者:中华医学会骨质疏松和骨矿盐疾病分会 我要说
来源:中华骨质疏松和骨矿盐疾病杂志2020年11月第13卷第6期
摘要
骨质疏松症已成为我国重要的公共健康问题。地舒单抗作为一种具有较广抗骨折谱的抗骨质疏松药物,在国外应用已超过10年,大量的临床证据显示其可持续增加绝经后骨质疏松症的骨密度,并降低椎体、非椎体及髋部骨折的风险。地舒单抗在国内上市为骨质疏松症的治疗提供了一种新“武器”,但我国临床工作者对地舒单抗的应用经验尚不多。为此,中华医学会骨质疏松和骨矿盐疾病分会组织专家,在充分复习汇总循证医学证据的基础上,对地舒单抗在骨质疏松症中的临床合理用药提出建议,以供参考。
关键词:地舒单抗; 骨质疏松症; 骨密度; 骨折
骨质疏松症是一种以骨量减少,骨组织微结构破坏,导致骨脆性增加,易发生骨折为特征的全身性疾病[1]。骨质疏松症多见于绝经后女性和老年男性,也可发生于任何年龄。我国50岁以上女性人口已达2.3亿[2],而该年龄段女性骨质疏松症患病率高达32.1%。因此,骨质疏松症已成为我国面临的重要公共健康问题。
2017年,中华医学会骨质疏松和骨矿盐疾病分会更新了《原发性骨质疏松症诊疗指南( 2017) 》[3]。对有抗骨质疏松药物使用适应证的患者,指南推荐首选具有较广抗骨折谱的药物,主要为骨吸收抑制剂(如阿仑膦酸钠、唑来膦酸、利塞膦酸钠和地舒单抗等); 对高骨折风险者,推荐使用唑来膦酸、特立帕肽或地舒单抗等治疗。
地舒单抗( denosumab) 是一种全人源单克隆抗体(IgG2类),以高特异性和高亲和力与核因子-κB受体活化因子配体[receptor activator of nuclear factor-κB ( NF-κB ) ligand,RANKL]结合,阻止RANKL与其受体核因子-κB受体活化因子( receptor activator of nuclear factor-κB,RANK) 结合,从而抑制破骨细胞形成和活化。地舒单抗是目前唯一上市的RANKL抑制剂,于2010年首次在欧盟上市被批准用于治疗骨折高风险的绝经后女性和男性骨质疏松症,于2020年6月在我国获批上市。
地舒单抗在国内的上市为骨质疏松症的治疗提供了一种新的“武器”。我国临床工作者对地舒单抗的应用经验尚不多。为此,本会对地舒单抗在抗骨质疏松症治疗中的作用机制、循证医学证据、应用注意事项等提出合理用药建议(建议要点见表1),以供临床参考。
表1 地舒单抗在骨质疏松症合理用药的建议要点



RANKL/RANK/OPG 信号通路及地舒单抗的作用机制
正常生理状态下,骨形成与骨吸收保持动态平衡,去除旧骨、合成新骨的过程被称为骨重建(bone remodeling) ,保证了骨组织的不断更新及损伤的修复。骨质疏松症的主要发病机制是骨重建失衡,即骨吸收超过了骨形成。RANKL /RANK/OPG 信号通路是调节破骨细胞分化、活化及功能的关键信号通路[4]。RANK 属于I型跨膜蛋白,是肿瘤坏死因子受体(tumor necrosis factor receptor,TNFR) 超家族成员之一。RANK高度表达于许多细胞的表面,如破骨细胞前体细胞、成熟破骨细胞等。RANKL是RANK 的配体,主要由成骨细胞和活化的T淋巴细胞表达,有膜结合型和分泌型两种类型。大多数促进破骨细胞形成和分化的因子均可诱导成骨细胞表达和分泌RANKL。RANKL与破骨细胞前体细胞表面的RANK 结合,通过RANK 的胞内信号通路诱导激活NF-κB,调控破骨细胞分化相关基因的
表达,促进破骨细胞的分化成熟和活化。成骨细胞分泌的骨保护素(osteoprotegerin,OPG) ,可作为分泌型RANKL的受体,与RANK竞争性结合RANKL,从而抑制破骨细胞的生成和活化[5]。RANKL/OPG的比值直接影响骨吸收。因此,RANKL /RANK/OPG信号通路对调节骨重建有重要作用,也是抗骨质疏松药物研发的重要靶点。
地舒单抗是目前可用于人体治疗的活性最强的RANKL抑制剂。其以高亲和力与RANKL结合,抑制RANKL与RANK的相互作用,抑制破骨细胞的生成与功能(图1),从而减少骨吸收、增加骨量、改善骨强度[6]。地舒单抗对RANKL的结合具有高度特异性,目前未发现其与TNF家族的其他成员( 如TNFα、TNFβ 等) 结合[7]。
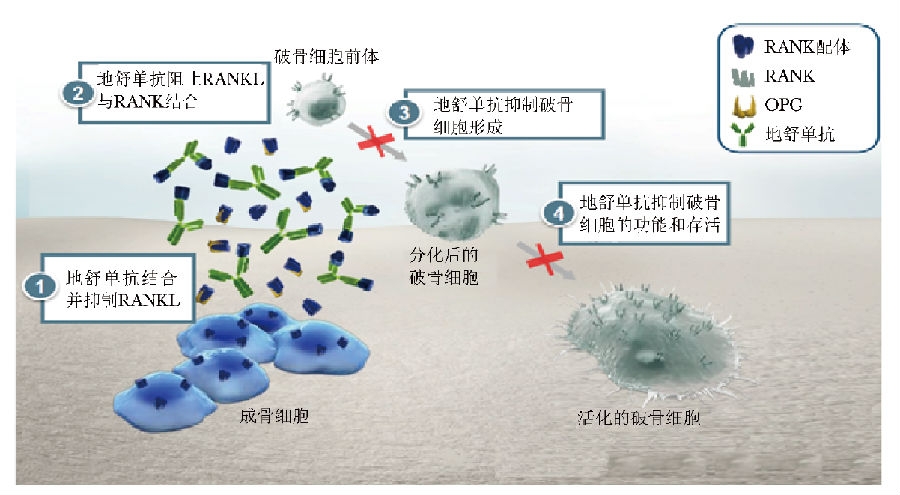
图1 地舒单抗的作用机制
地舒单抗的药代药效动力学
药代动力学
地舒单抗60mg皮下注射后,在第10天(范围2 ~ 28 d) 达到最大血清浓度(Cmax) ,Cmax为6μg /mL(范围1~17μg /mL) ,达到Cmax之后,血清水平在3个月( 范围1.5 ~ 4.5个月) 内逐渐下降,半衰期为26d(范围6 ~ 52 d) 。每6个月一次60mg用药后,未观察到地舒单抗的累积或药代动力学特征随时间推移而变化,且男性与女性之间的药代动力学相似。年龄(28 ~ 87 岁) 、人种和疾病状态未显示对地舒单抗的药代动力学有显著影响。在一项针对不同肾功能受损程度的患者(包括接受透析的患者) 的研究中,肾功能受损程度对地舒单抗的药代动力学无影响。未专门在肝功能损害患者中对地舒单抗的药代动力学进行研究,一般而言,单克隆抗体不经肝代谢清除,推测肝功能损害对地舒单抗药代动力学无影响。
药效动力学
临床研究显示,地舒单抗60mg皮下注射可迅速降低骨转换速率,骨吸收标志物血清I型胶原羧基末端肽交联(C-terminal telopeptide of type 1 collagen,CTX) 水平可在给药后第3天下降约85%,1个月内下降至最低。在每个给药间隔结束时,
CTX水平部分回升,从最大下降≥87%回升至下降≥45% (范围45%~80%) ,反映了当血药浓度降低时地舒单抗对骨重建影响是可逆的。停用地舒单抗并且无后续治疗的情况下,骨吸收标志物会反弹性升高,甚至超过基线水平40%至60%,但在12个月内回到基线水平。因此,持续治疗才能够维持地舒单抗对骨吸收的长期抑制[8]。
地舒单抗的临床有效性
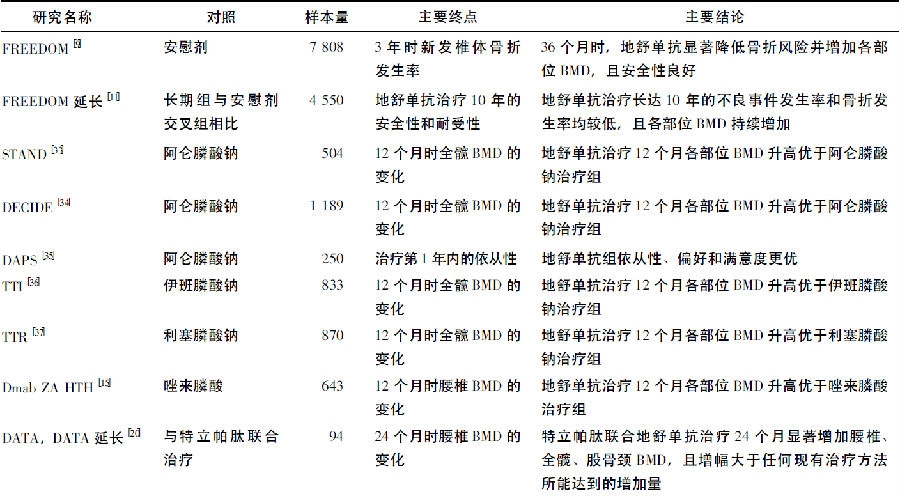
地舒单抗在国外应用已超过10年,积累了较丰富的临床证据(附录1) 。目前全世界已完成10余项关于地舒单抗的临床研究,其中规模最大的是FREEDOM 3年研究及其10年延长研究,FREEDOM研究为地舒单抗的临床疗效和安全性提供了重要证据。
FREEDOM 3年研究是一项随机、双盲、安慰剂对照的Ⅲ期临床试验,用于评价地舒单抗在绝经后骨质疏松症妇女中的疗效和安全性[9]。研究共入组了7808例60~90岁绝经后骨质疏松症女性,将受试者随机分配至地舒单抗60mg治疗组或安慰剂组,每6个月一次皮下注射,连续治疗36个月。结果显示: 36个月后,地舒单抗组腰椎BMD增幅较安慰剂组升高9.2%(95% CI: 8.2%~10.1%) ,地舒单抗组全髋BMD增幅较安慰剂组升高6.0%(95% CI: 5.2%~6.7%) ; 与安慰剂组相比,地舒单抗治疗可降低影像学诊断的新发椎体骨折风险68%、髋部骨折风险40%以及非椎体骨折风险20%。
对纳入FREEDOM 3年研究的骨折高风险绝经后骨质疏松症女性(已存在多发或中重度椎体骨折,或年龄≥75岁,或股骨颈BMD T值≤-2.5)进行亚组分析,结果显示: 与安慰剂组相比,地舒单抗治疗可显著降低既往椎体骨折的骨质疏松症女性的新发椎体骨折风险55%; 显著降低年龄≥75岁的骨质疏松症女性的髋部骨折风险62%; 也可以显著降低基线股骨颈BMD T 值≤-2.5的女性髋部骨折风险47%[10]。
在FREEDOM 3年研究结束后,将4550例受试者继续纳入为期7年的开放标签延长研究中,均接受地舒单抗60mg每6个月一次皮下注射治疗[11]。最后,治疗组1343例(共接受地舒单抗治疗10年,长期组)、安慰剂组1283 例(共接受地舒单抗治疗7年,交叉组) 完成了后续7年延长研究。结果显示: 研究完成时,长期组受试者的腰椎、全髋、股骨颈和桡骨1/3 处BMD较FREEDOM研究基线时分别增加了21.7%、9.2%、9.0%和2.7%; 交叉组受试者的腰椎、全髋、股骨颈和桡骨1/3处BMD较延长研究基线时分别增加了16.5%、7.4%、7.1%和2.3%。在这7年间,新发椎体骨折和非椎体骨折的年发生率均保持在较低水平,分别为0.90%~1.86% 和0.84%~2.55%,低于虚拟的长期安慰剂队列的预计发生率。
上述研究结果显示,地舒单抗可持续增加绝经后骨质疏松症患者的BMD,并降低其椎体、非椎体及髋部骨折的风险,特别可以降低骨折高风险患者椎体和髋部骨折的发生率。国内外绝经后骨质疏松症诊疗指南已将地舒单抗作为抗骨吸收类药物的推荐之一(附录2) 。
地舒单抗临床使用方案
地舒单抗的国内、外适应证
地舒单抗在欧盟和美国5个方面获批适应证,分别为: (1)治疗高骨折风险绝经后妇女骨质疏松症; (2)治疗高骨折风险男性骨质疏松症,以增加骨量; (3)治疗高骨折风险男性和女性糖皮质激素诱导的骨质疏松症; (4)接受雄激素剥夺疗法的高骨折风险非转移性前列腺癌男性,以增加骨量; (5) 接受芳香化酶抑制剂疗法的高骨折风险乳腺癌女性,以增加骨量[8]。
地舒单抗在中国于2020年6月获批的适应证为: 用于骨折高风险的绝经后妇女的骨质疏松症。在绝经后妇女中,本品可显著降低椎体、非椎体和髋部骨折的风险。
关于适应证中“骨折高风险”的说明
参考国际上相关指南[12-13],可将“极高骨折风险”定义为确诊骨质疏松症且满足以下任何一项者: (1)过去2 年内发生过脆性骨折; (2)接受抗骨质疏松药物治疗时发生脆性骨折; (3)多发性脆性骨折; (4)正在使用可导致骨骼损伤的药物(如长期接受糖皮质激素治疗);(5)BMD T值极低的患者(如T值<-3. 0);(6)高跌倒风险或有跌伤史; (7) FRAX 或其他确认的算法估算为极高骨折风险(如FRAX 预测未来10年主要骨质疏松性骨折风险>30% 或髋部骨折风险>4.5%) 。确诊骨质疏松症,但不存在极高骨折风险者为高骨折风险患者。值得注意的是,存在极高骨折风险的患者应采取更积极的治疗,让患者的骨折风险维持在可接受的范围内。
地舒单抗的使用方法、禁忌证和使用前注意事项
使用方法: 建议剂量60mg,每6个月在大腿、腹部或上臂经皮下注射1次。
禁忌证: (1)对活性成分或任何辅料成分过敏者禁用; (2)低钙血症。
使用前注意事项: 在开始治疗前必须摄入足够的钙和维生素D 以防止发生低钙血症。推荐在每次给药前,以及在易于出现低钙血症的患者于首次给药后2 周内,对其血钙水平进行临床监测。若患者在治疗期间出现低钙血症疑似症状,应测定血钙水平。
临床应用中的若干问题
地舒单抗注射以后多长时间起效,治疗过程中如何监测疗效?
地舒单抗60mg注射以后,血清CTX水平在第3天下降约85%,1个月左右达到最大下降幅度[8]。证据显示地舒单抗治疗6个月时,患
者腰椎、全髋和股骨颈的BMD 显著增加[9]。建议在开始治疗前检测BTM 和基于DXA的BMD基线值,开始治疗后第1个月、第3~6个月再
次检测BTM了解治疗反应,每年检测1次椎体和髋部BMD 以监测疗效[14]。
肾功能不全患者如何使用?
肾功能不全的患者不需要调整剂量,但重度肾功能损害患者(肌酐清除率<30 mL /min) 或接受透析的患者发生低钙血症的风险更高。因此,摄入足够的钙、维生素D和定期监测血钙水平对这类患者尤其重要。
既往使用过双膦酸盐的患者是否可以转换成地舒单抗治疗?
使用双膦酸盐治疗的患者可以转换成地舒单抗治疗,特别是如下情况可考虑转换:(1)肾功能不全; (2)不能耐受双膦酸盐类的不良反应;(3)对口服双膦酸盐依从性不佳; (4)双膦酸盐治疗过程中发生新的脆性骨折。临床研究证据显示,既往使用过阿仑膦酸钠、利塞膦酸钠、伊班膦酸钠或唑来膦酸的患者转换成地舒单抗治疗后,各部位BMD 可进一步升高[15-17]。
双膦酸盐能够与地舒单抗联合应用吗?
双膦酸盐与地舒单抗同为骨吸收抑制剂,不建议联合使用。
已进入双膦酸盐药物假期的患者能否序贯地舒单抗治疗?
对于已进入双膦酸盐药物假期的患者,应每年评估患者病情,包括年龄、跌倒史、是否有新的骨折、可能危险因素、BMD和BTM。双膦酸盐药物假期期间,如果发生新的骨折、骨折风险增加、腰椎或髋部BMD下降≥4%或腰椎和髋部BMD同时下降,应重启抗骨松治疗,地舒单抗是重启治疗的药物选择之一[18-19]。
特立帕肽能否与地舒单抗序贯或联合治疗?
特立帕肽的使用时间不应超过2年,停药后应尽快序贯使用骨吸收抑制剂,以维持特立帕肽所取得的疗效[12]。DATA系列研究结果显示,特立帕肽治疗2年后,序贯地舒单抗治疗能显著提高腰椎、全髋和股骨颈BMD。但地舒单抗治疗两年后序贯特立帕肽治疗,患者髋部BMD在12个月内会显著降低,之后再逐渐升高。特立帕肽与地舒单抗联合治疗较特立帕肽或地舒单抗单药治疗提升各部位BMD 更加显著[20-21]。DATA系列研究的主要终点是BMD变化,特立帕肽序贯或联合地舒单抗治疗的抗骨折疗效尚需进一步研究。
地舒单抗可以持续用多久? 是否有药物假期?
患者使用地舒单抗治疗5 ~10年后应重新评估骨折风险,对于仍然处于骨折高风险的患者,可继续地舒单抗治疗或换用其他抗骨质疏松药物。对于骨折低风险的患者可考虑转换成双膦酸盐继续治疗。地舒单抗长期治疗可持续提升各部位BMD,无平台期。与双膦酸盐类药物的作用机制不同,地舒单抗不会在骨基质中沉积,其抑制骨转换的作用具有可逆性,停药后BMD在1~2年内回落至治疗前水平,骨折风险升高,因此地舒单抗的使用没有“药物假期”的概念[12, 22]。
地舒单抗停药以后如何序贯治疗?
目前一些研究显示,停用地舒单抗后可出现骨吸收增加、BMD回落至治疗前水平、多发性椎体骨折风险增加,特别是在既往发生过椎体骨折的患者中[23-24]。有研究显示,停用地舒单抗后序贯使用阿仑膦酸或唑来膦酸可部分减缓这种BMD下降[25-26]。在应对地舒单抗停药后BMD下降、骨折风险增加方面,尚需更多的研究去探索最佳的序贯治疗方案。对于正在接受地舒单抗治疗的患者,不应随意停药。若因各种原因需要停用地舒单抗,建议转换至其他抗骨吸收药物治疗(如双膦酸盐) 以减缓BMD下降及骨折风险增加,并需密切监测BTM及BMD的变化。
如果漏用了一剂,该如何处理?
为确保治疗效果,每6个月定期接受一次地舒单抗治疗非常重要。如果遗漏一剂地舒单抗,应尽快补充注射。此后,应从末次注射之日起每6个月注射一次[8]。
地舒单抗是否会影响骨折愈合?
在FREEDOM 研究中,因非椎体骨折接受手术治疗的患者未发现地舒单抗影响骨质疏松症患者骨折的愈合[27]。
骨折手术围手术期使用地舒单抗是否增加手术并发症或术后感染的风险?
FREEDOM研究表明地舒单抗在骨折围手术期间使用,不会增加手术并发症或者术后感染的风险[27]。
地舒单抗对骨折手术植入物有何影响?
地舒单抗对骨质疏松性骨折手术植入物的影响,尚未有大样本循证医学研究。有小规模临床研究表明,老年骨质疏松症患者全髋关节置换术后两周内启用地舒单抗治疗,一年后假体周围骨量较安慰剂组增加[28]; 尚缺乏地舒单抗降低假体松动发生率、提高假体置换手术疗效的长期证据。
现有研究结果提示: 在没有禁忌证、充分补充钙剂和维生素D并且血钙水平正常的情况下,骨质疏松性骨折患者可随时启动地舒单抗进行抗骨质疏松症治疗。
临床应用中安全性及处理原则
FREEDOM 3年研究显示,在不良事件和严重不良事件的总发生率方面,地舒单抗治疗组与安慰剂组间无显著差异。10年延长研究同样显示了良好的长期治疗安全性。在FREEDOM 3年研究和10年延长研究中,无受试者检测出产生抗地舒单抗的中和抗体[9,11]。在患者接受地舒单抗治疗过程中,需要关注的安全性问题汇总如下。
地舒单抗的主要不良反应有哪些?
地舒单抗最常见的不良反应包括肌肉骨骼疼痛和肢体疼痛; 偶见蜂窝织炎病例; 罕见低钙血症、超敏反应、颌骨坏死和非典型股骨骨折病例。
地舒单抗会增加患者感染的风险吗? 使用免疫抑制剂的患者是否可以使用?
FREEDOM 3年研究显示,地舒单抗组的严重感染住院率要高于安慰剂组,主要为蜂窝织炎。在10年延长研究中,地舒单抗组患者蜂窝织炎的发生率并没有增加,与安慰剂组发生率相当; 且机会性感染的发生率及所有感染的总体发生率也与安慰剂组相似[9]。在针对糖皮质激素诱导的骨质疏松症( glucocorticoid-induced osteoporosis,GIOP) 患者的Ⅲ期临床研究中,与利塞膦酸钠相比,地舒单抗在GIOP 患者中没有增加感染及严重感染的风险[29]。
地舒单抗会引起低钙血症吗? 该如何避免?
在FREEDOM 3年研究中,所有患者每天至少补充1000mg元素钙,基线血清25羟维生素D浓度为12~20ng/mL的患者每天补充至少800IU维生素D,基线25羟维生素D浓度大于20ng/mL的患者每天补充至少400IU维生素D。研究过程中,地舒单抗组有4例受试者血清总钙水平降至2.0 mmol/L以下,但安慰剂组也有5例受试者出现该情况,提示地舒单抗并不会增加普通绝经后骨质疏松症女性发生低钙血症的风险。对于存在低钙血症危险因素的患者,比如严重肾功能不全甚至透析的患者,地舒单抗治疗存在诱发或加重低钙血症的潜在风险[30-31]。因此,建议在应用地舒单抗前,需对患者血钙水平进行评估,已经出现低钙血症的患者要先纠正低钙血症。所有接受地舒单抗治疗的患者,需同时补充足量的钙剂和维生素D,在治疗期间需要监测血钙水平。
地舒单抗会引起颌骨坏死吗? 该如何注意?
在FREEDOM 3年研究中,地舒单抗治疗组未发现颌骨坏死病例。在10年延长研究中,累积发生13例颌骨坏死病例,暴露校正受试者发生率(exposure-adjusted participant incidence) 为5.2例/10000受试者年[11],属于罕见的不良反应。颌骨坏死的风险可能会随着地舒单抗治疗时间的延长而增加。建议开始地舒单抗治疗前,对需要进行侵入性牙科治疗的患者给予提醒。治疗期间,嘱患者保持良好的口腔卫生习惯,非必要应避免进行侵入性牙科治疗,如必须行牙科手术应避免临近地舒单抗给药时间,并经由专科医师评估[32]。
地舒单抗会导致非典型股骨骨折吗?
在FREEDOM 3年研究中,地舒单抗治疗组未发现非典型股骨骨折病例。在10年延长研究中,长期组和交叉组各有1例非典型股骨骨折病例,暴露校正受试者发生率为0.8例/10000受试者年,属于极罕见的不良反应[11]。建议嘱患者在用药期间需注意有无大腿、髋部或腹股沟疼痛症状,若有上述症状,需进一步评估是否发生了非典型股骨骨折。
附录1 地舒单抗在绝经后骨质疏松症的临床研究

附录2 国内外指南对地舒单抗的推荐

参考文献










 京公网安备11010502051256号
京公网安备11010502051256号