我们能像蝾螈那样再生吗?
2016-12-15 作者:解放军空军总医院骨科 厉晓杰 我要说
电影里很多超级英雄都拥有令人羡慕的再生能力。现实世界里,很多动植物均具有再生的能力。但在脊椎动物中,能进行复杂肢体再生的四足动物只有蝾螈。成年哺乳动物的再生能力多数情况下仅限于指尖的再生。
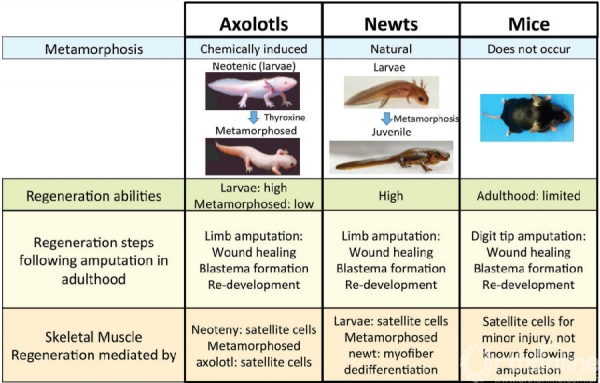
美西钝口螈(Axolotls)和红绿东美螈(Newts)是最常用作研究的两种蝾螈。它们都具有强大再生能力,但又有一定的区别。Newt自然条件下可以进行变形发育,而Axolotls诱导后才能变形发育,变形发育后肢体再生能力显著下降。
尽管两种蝾螈的生长周期不同,但是二者在肢体再生时经历相同的三个过程:创伤修复、芽基形成和重建。
创伤修复
蝾螈被截肢后,角质细胞迁移并包裹伤区,形成多层创伤表皮,神经的长入后,形成“信号中心”,也称为顶端上皮帽(AEC)。AEC与剩余细胞发生直接联系,通过多种途径调控肢体再生过程。AEC能提供多种信号分子,包括FGF、BMP、TGF-β、IGF和Wnt等。免疫应答在防止创伤瘢痕形成过程中也起到了至关重要的作用。去除巨噬细胞后,大量成纤维细胞分化成为肌成纤维细胞,后者具有较高的促纤维形成活性导致瘢痕愈合。
引起瘢痕形成的因素涉及神经支配、炎症反应和成纤维细胞分化等多方面。通过对比研究蝾螈和人类,可能在未来能探索出促进无瘢痕愈合及肢体再生的药物。
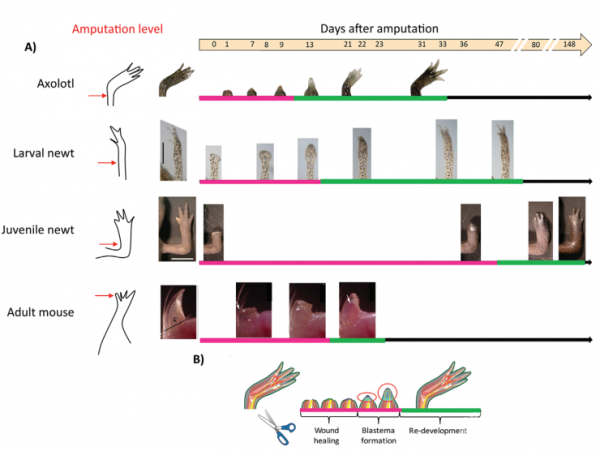
芽基形成
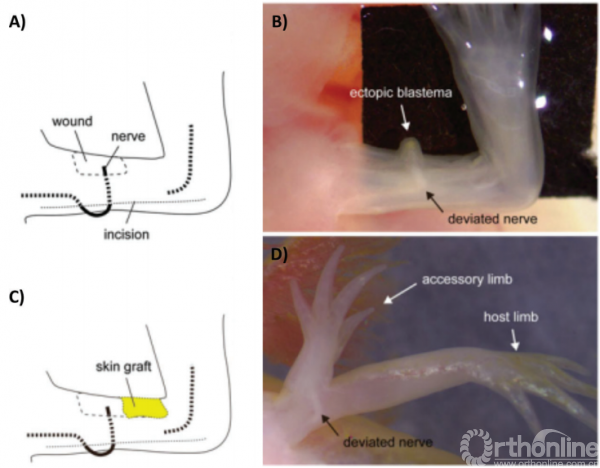
芽基是由未分化细胞和增殖细胞构成的生长区,再生组织和肢体均由此生成。AEC募集细胞并促进了细胞的去分化,进而形成芽基。芽基可自发形成缺失结构,将成熟芽基移植到其他位置,不论移植位置为何,均能发育出原缺失结构。
位置信息在肢体再生过程中至关重要。皮肤含有位置信息,通过表观遗传学方式储存在成纤维细胞中。脊椎动物发育过程中每个细胞的空间的位置信息多由三个坐标轴确定:前后轴(AP)、近远轴(PD)和背腹轴(DV)。FGF8与SHH在AP轴发育中具有调控作用,但具体的发育调控机制仍需要进一步的研究。芽基的形成并不局限于蝾螈中,在部分哺乳动物再生过程中也有发现。对哺乳动物和蝾螈的再生过程进行对比研究,可能发现一些促进芽基形成的信号通路。
重塑
芽基的生物学行为与胚胎发育过程中的肢芽相像。因此推测再生过程中细胞的迁移、增殖和分化的调控机制与胚胎发育相似。再生过程中的位置信息涉及含有同源异形盒基因的表达,如HoxA9, HoxA11和Hoxa13。尽管如此,将无瘢痕修复应用到哺乳动物上,仍然有很长的路要走。
TGF-β1与纤维化
再生过程中巨噬细胞起到重要作用,巨噬细胞分泌的TGF-β1促进了成纤维成脂祖细胞的存活,后者分化为肌成纤维细胞,进而形成纤维性瘢痕。蝾螈和哺乳动物再生过程中TGF-β1水平的区别是导致愈合结果不同的原因之一。
Wnt信号与芽基形成
不论成年人还是小鼠,都保留一定程度的再生能力。研究表明,WNT信号配体能够促进成体小鼠和蝾螈的皮肤和毛囊修复。Wnt信号释放活性因子吸引神经进而促进再生。哺乳动物再生能力局限很大一部分由于再生部位局部信号通路级联反应受损,而不是缺少再生过程所需细胞。
Rb/ARF/p53轴与骨骼肌细胞去分化
Rb具有调控细胞周期和DNA合成的作用。Rb表达下调可导致C2C12肌管细胞去分化并重新进入细胞周期。P19/ARF与Rb基因具有协同作用,在哺乳动物细胞中广泛表达,但是在C2C12成肌细胞和两栖动物中不表达。P19/ARF是Rb信号的下游信号,能够隔离p53的抑制因子MDM2,从而促进p53的转录。P53水平在蝾螈芽基形成时一过性下降,促进细胞重新进入细胞周期。药物干预哺乳动物Rb和p19/ARF可能促进肌纤维细胞去分化,形成成肌细胞促进肢体再生。
展望
蝾螈是一种终生都能保持肢体再生能力的神奇生物,哺乳动物也保存了很有限的肢体再生能力,并与蝾螈肢体再生存在一定的相似性。这就为蝾螈再生研究点亮了用于人类的希望。通过对比二者的不同可能为人类带来促进肢体再生的新疗法。


 京公网安备11010502051256号
京公网安备11010502051256号