3D打印多孔支架用于高感染风险骨缺损的修复
2017-05-25 作者:上海交通大学医学院附属第九人民医院骨科 杨颖 于志锋 我要说
在骨科临床上,大段的骨缺损常伴有伤口的污染或开放,存在较高的感染风险。植入的材料在某种程度上也创造了细菌粘附生长的载体或微环境,细菌可在其表面形成生物膜,而生物膜的形成是感染发生的关键环节。近期,上海交通大学医学院附属第九人民医院骨科汤亭亭教授团队利用3D打印方法,制备了聚乳酸-羟基乙酸共聚物/羟基磷灰石(PLGA/HA)复合多孔生物支架并表面接枝壳聚糖季铵盐(HACC);体内外研究表明,该人工骨组织修复支架不仅具有很好的成骨能力,还兼具良好的抗菌活性。由于目前大多数骨缺损修复材料或技术都只着眼于无菌环境下的骨修复;此种兼具抗菌性能的人工骨组织替代材料,对临床上高感染风险或已感染骨缺损的防治具有重要应用价值。
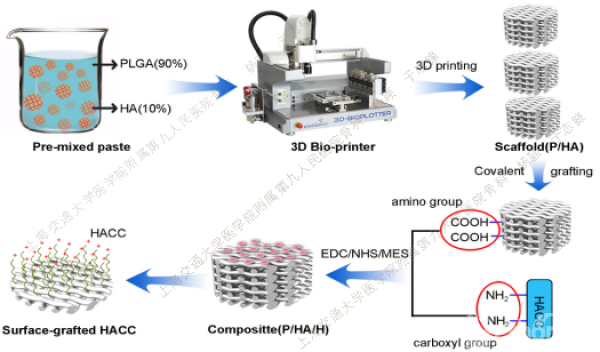
Fig.1. Schematic illustration for the synthesis of PLGA/HA/HACC composite porous scaffolds.
如图1所示,研究人员首先利用3D打印技术制备多孔立体PLGA/HA支架,然后将课题组前期研发的具有显著抗菌活性的HACC以共价键结合的方式接枝于复合支架材料上。该3D打印支架的孔隙率为80%左右,孔隙连通率接近100%,孔径为320μm左右(图2);接枝的HACC可随支架材料的降解而缓慢释放,4周模拟体液浸泡后,HACC总缓释量等于其初始负载量的70%左右。

Fig.2. Morphological characterization of 3D-printed composite scaffolds. (a) 3D reconstructed images ofthe scaffolds obtained using micro-CT; (b) Representative SEM images of the porous, composite scaffolds.
研究人员随后将打印的支架材料分为四组(P:单纯PLGA;P/HA:PLGA-HA;P/H:PLGA-HACC;P/HA/H:PLGA-HA-HACC)开展体外细菌学和细胞学试验。首先通过金葡菌及其耐药菌株接种及死/活细菌染色发现,接枝HACC的支架(P/H和P/HA/H)均可显著抑制细菌的早期粘附和生物膜形成(图3)。
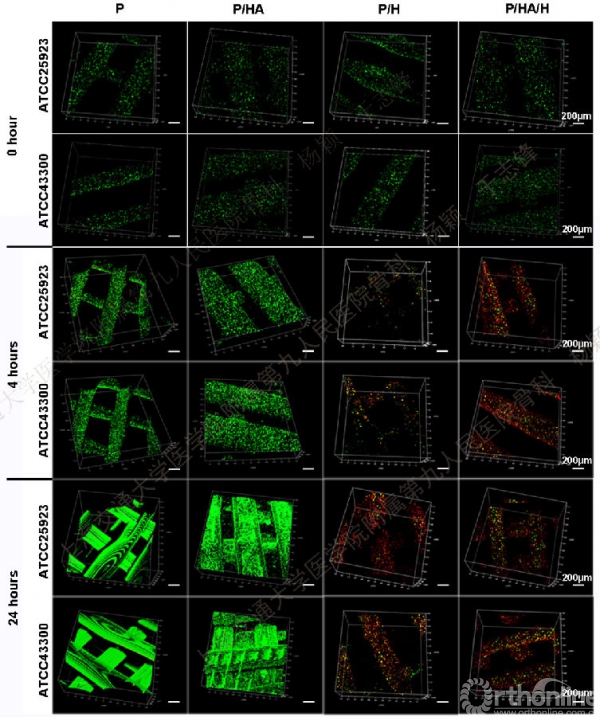
Fig.3. Three-dimensional images of bacterial viability on the surfaces of various scaffolds at 4 h and 24 h obtained using confocal laser scanning microscopy (CLSM) after the scaffolds were stained with the BacLight dead/live stain.
研究人员进一步观察了各组支架表面人骨髓间充质干细胞(hBMSCs)的粘附、增殖、骨架铺展和凋亡情况。实验结果表明,掺有羟基磷灰石的支架材料(P/HA和P/HA/H组) 表现出良好的细胞相容性,干细胞在其表面有更好的铺展和增殖。成骨分化试验表明,含羟基磷灰石的两组支架材料表现出了更显著的成骨活性,且支架表面接枝的HACC对支架的成骨性能无不利影响(图4)。
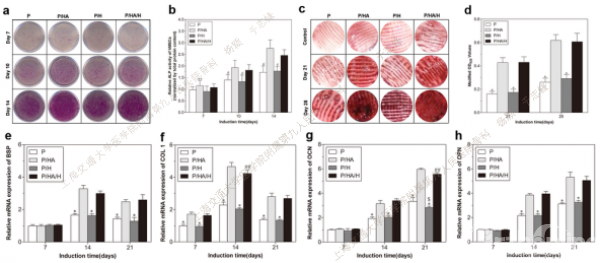
Fig.4. Osteogenic differentiation evaluation of various scaffolds. (a) ALP staining after osteogenic induction for 7, 10 and14 days. (b) Quantitative analysis of ALP activity. (c) Alizarin-red staining and (d) its quantitative analysis after 21 and 28 days induction. Relative mRNA expression of osteogenic differentiation-related genes in hBMSCs grown on various of scaffolds measured by real-time PCR after 7, 14 and 21 days induction: (e) BSP, (f) COL 1, (g) OCN and (h) OPN.
同时,研究人员还利用生物发光金葡菌建立了动物皮下感染模型,实时、持续观察了各组支架表面负载细菌在体内的生长情况,发现支架表面接枝HACC后,可有效抑制皮下植入物感染的进展,发挥了较好的体内抗菌活性(图5)。进一步的组织学分析显示,表面接枝了HACC的支架孔隙内的脓性病灶、炎性细胞浸润、炎性纤维化和细菌残留等均要显著低于其余两组,表明负载有HACC的复合多孔支架能有效发挥体内抗菌性能。
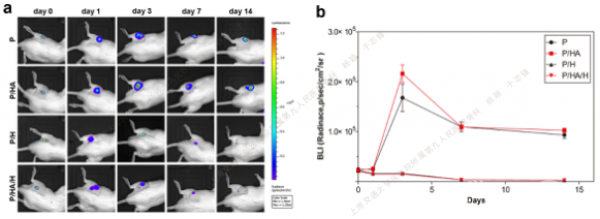
Fig.5. Real-time monitoring of bacterial photon intensity detection from metabolically active S.aureus Xen29 in the subcutaneous embedding model. (a) Representative images of in vivo bioluminescence over a period of 14 days using an IVIS camera. (b) Curves of mean bacterial burden.
综上所述,该研究中制备的复合支架能显著抑制细菌粘附和生物膜形成,进而有效阻止感染的发生和发展;同时还能促进干细胞的粘附、增殖、骨架铺展和成骨分化,具有良好的细胞和组织相容性。课题组近期还完成了高感染风险原位骨缺损修复动物模型的研究,证实此抗菌支架可以促进大鼠股骨感染性骨缺损的修复。
主要研究结果已于2016年9月26日在线发表于Acta Biomaterialia。论文的第一作者为汤亭亭教授的博士生杨颖同学,合作对象包括华东理工大学张洪波教授、香港中文大学秦岭教授、瑞士AO研究所Geoff Richard教授等团队,项目的开展得到了上海市科学技术委员会(13JC1403900)、国家自然科学基金委(51361130034)和欧盟第七框架研究计划项目(Nos.604517)的支持。
论文信息:
Ying Yang, Shengbing Yang, Yugang Wang, Zhifeng Yu, Haiyong Ao, Hongbo Zhang, Ling Qin, Olivier Guillaume, David Eglin, R. Geoff Richards, Tingting Tang. Anti-infective efficacy, cytocompatibility and biocompatibility of a 3D-printed osteo- conductive composite scaffold functionalized with quaternized chitosan. Acta Biomaterialia. 2016. 46: 112-128.


 京公网安备11010502051256号
京公网安备11010502051256号