弥漫性巨细胞瘤——昨天、今天和明天
2017-04-05 文章来源:骨科在线编委 复旦大学附属华山医院骨科 焦聚阳 夏军 陈飞雁 我要说
本文从腱鞘巨细胞瘤的前世今生,病因及机制、诊断、治疗等方便阐述弥漫性巨细胞瘤的昨天、今天和明天。
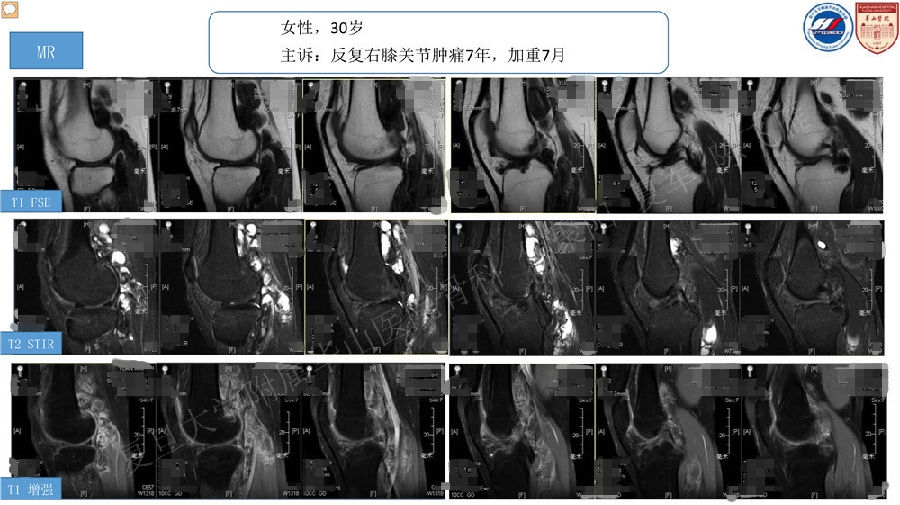
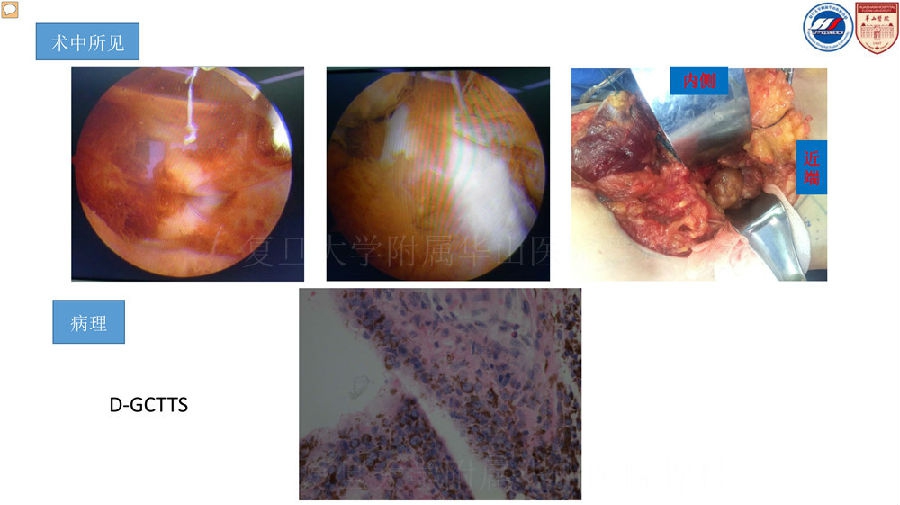



腱鞘巨细胞瘤的前世今生

腱鞘巨细胞瘤(Giant cell tumor of tendon sheath , GCTTS)
Localized of giant cell tumor (L-GCTTS)


WHO classification of tumoursof soft tissue and bone. Lyon: IARC Press; 2013. p 102-3.
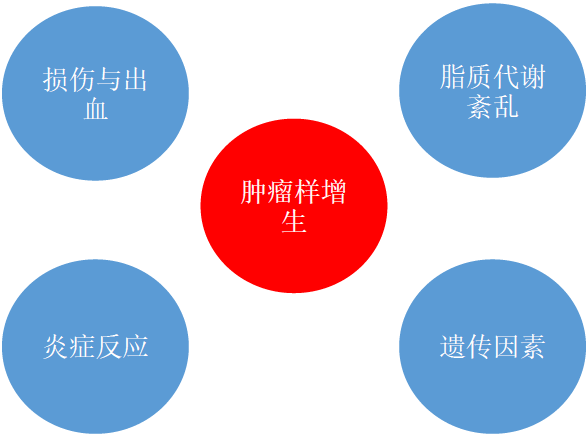
腱鞘巨细胞瘤的病因及可能的机制
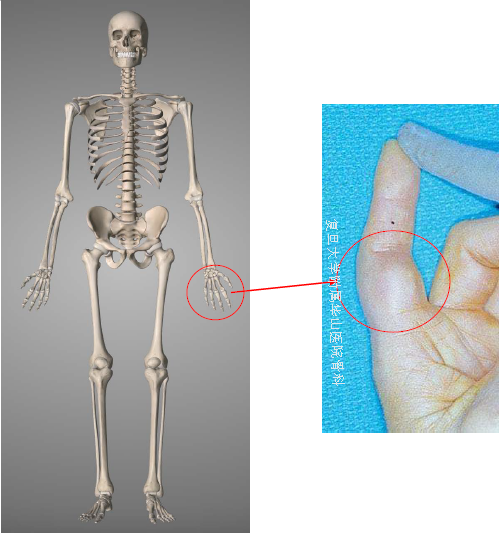
腱鞘巨细胞瘤的诊断
临床表现 L–GCTTS
1.年龄及性别分布:30-50yr,女:男=2:1
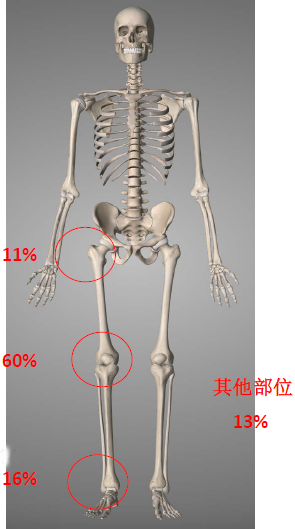
2.发生部位:手指(85%)(近腱鞘滑膜或指间关节);腕、踝/足、膝(少见);髋、肘(罕见)
3.主要症状:缓慢生长的坚实无痛性肿块(直径<3cm);
D–GCTTS(即PVNS)
1.年龄:较L-GCTTS更年轻(<40yr),
2.发生部位:
关节内——膝、踝/足、髋、肩;颞下颌关节、脊柱(罕见)
关节外——膝周、大腿和足
3.主要症状:肿胀(86%)、疼痛(82%)、僵硬(73%)、活动受限(64%)、关节不稳(64%);
PalmeriniE. et al, EurJ Cancer , 2014
Patient-reported Symptoms of TenosynovialGiant Cell Tumors,2016.4
影像学表现
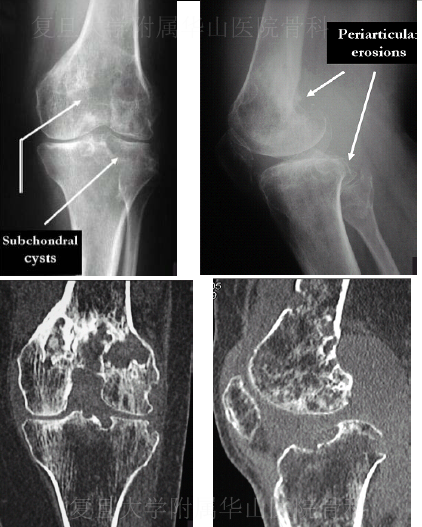
X-ray
早期正常
中期软组织肿胀
晚期关节周围骨侵蚀
L-GCTTS 15–25% D-GCTTS33-56%
软骨下骨囊肿
CT
关节周围骨侵蚀
软骨下骨囊肿
DPVNS 33%-50% 可见
软组织影
Kramer DE.J Knee Surg. 2009;22:243-254
MRI
含铁血黄素沉积——T1W低信号,T2W高低不等混杂信号
FS高信号,FSE晕状伪影(Blooming artifact)
MR增强:不均匀强化
特点
L-GCTTS:境界清楚、紧贴或包绕肌腱腱鞘生长的软组织肿块影
D-GCTTS:滑膜弥漫性增厚/多发软组织肿块影,境界不清

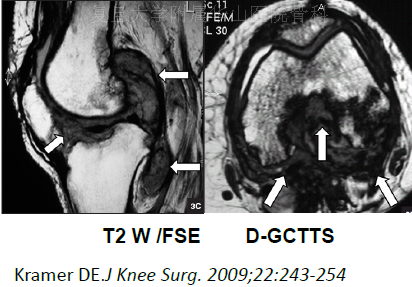
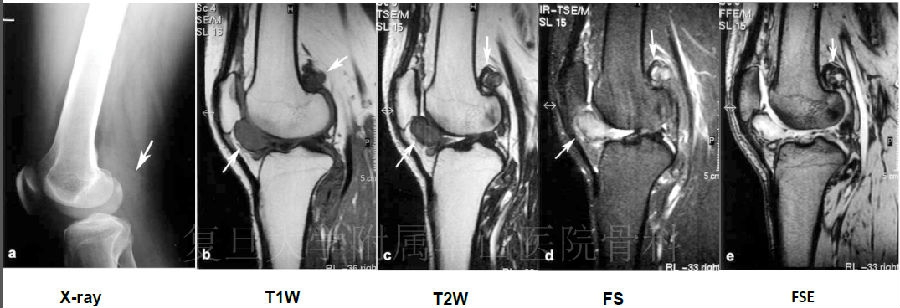
XiaoG,ClinRheumatol(2004) 23: 31–34
组织学表现
关节腔穿刺
75%血性、暗红色、棕红色25%黄色、黄褐色、暗褐色
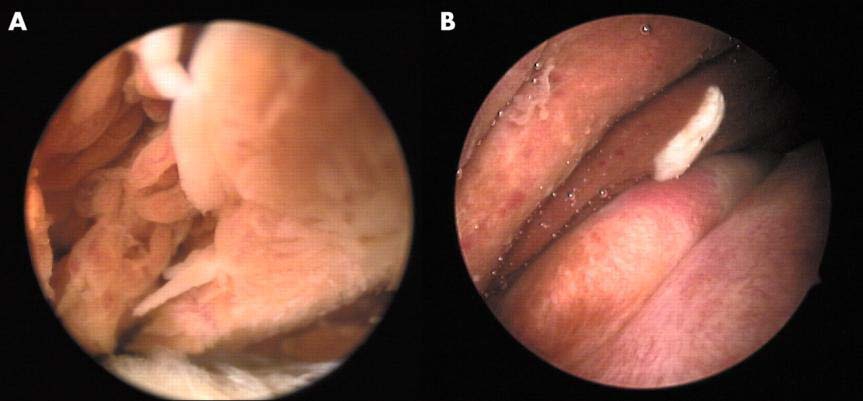
关节镜活检

L-GCTTS
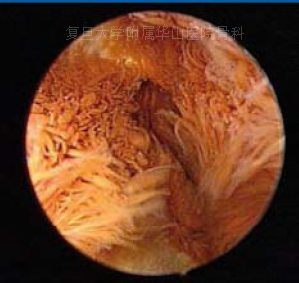
D-GCTTS
组织学表现 L-GCTTS
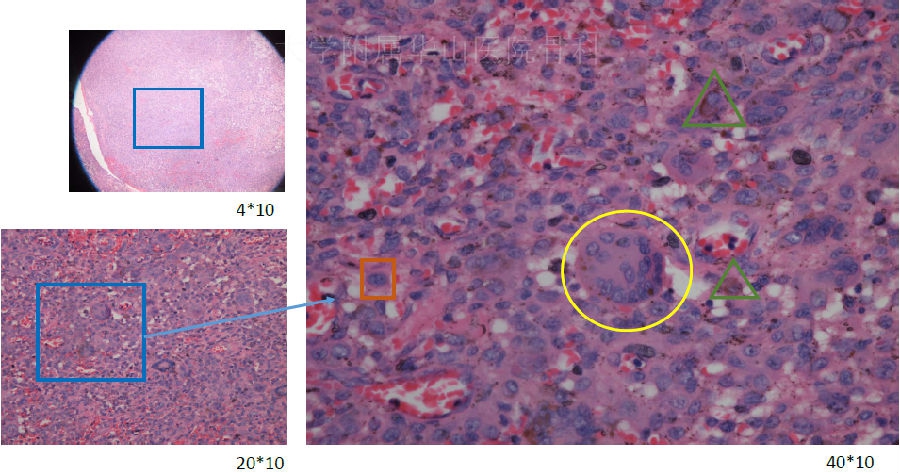
组织学表现 D-GCTTS
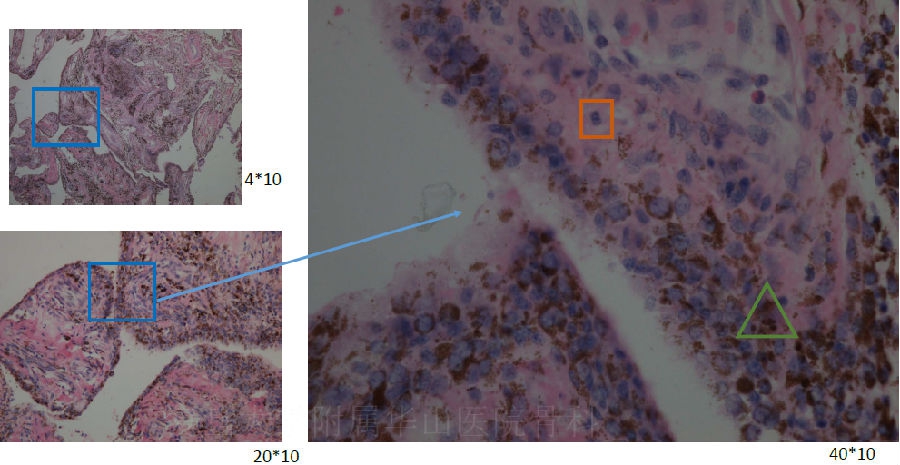
诊断

腱鞘巨细胞瘤的治疗
GCTTS的治疗
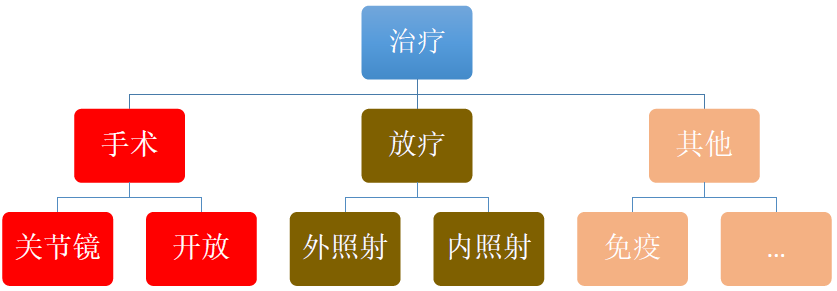
Pigmented VillonodularSynovitis A Comprehensive Review and Proposed Treatment Algorithm,JBJS REVIEWS 2016;4(7):e3
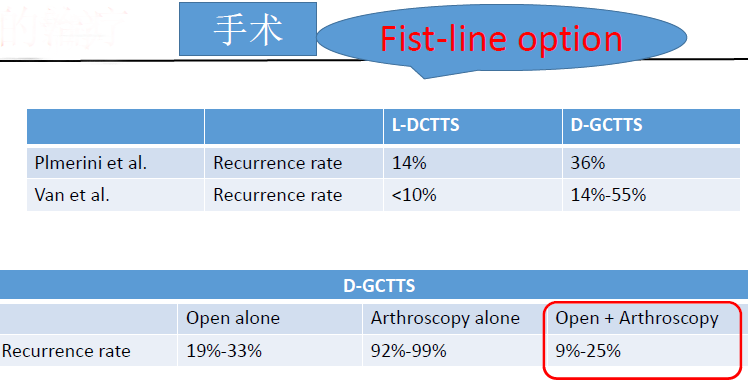
目前推荐:前方关节镜入路+后方开放入路
van der Heijden L et al. J Surg Oncol 2013;107(4):433e45. Stephen R et al.JBJS REVIEWS 2016;4(7):e3

并发症有:关节僵硬、关节功能丧失、肉瘤样变、皮肤反应、伤口愈合差、病理性骨折
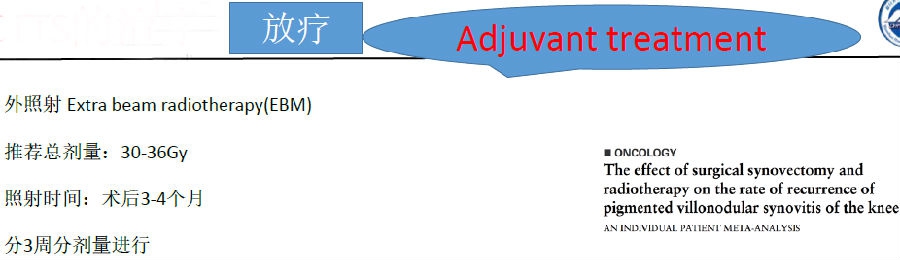
GCTTS的治疗 放疗
Case series(最大):73例(开放滑膜切除+术后)随访4.6年,膝GCTTS复发率:30%
并发症严重:放射性皮肤坏死、严重骨与软骨损伤;
关节外病变不适用
BickelsBJ JBJS (A) 2008



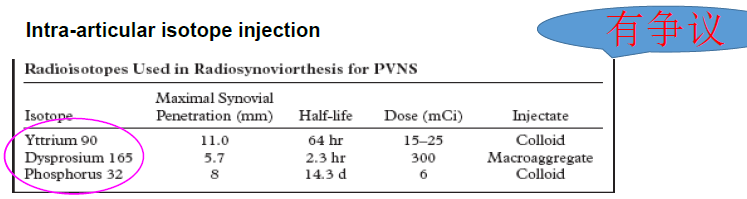
GCTTS的治疗 免疫疗法
病例报道:男20岁
开放性滑膜切除+ 90Y内放疗失败
关节镜标本:
TNF-a表达:
英夫利昔单抗
5mg/Kg
0-2-6-14-20w
2/mon---54W
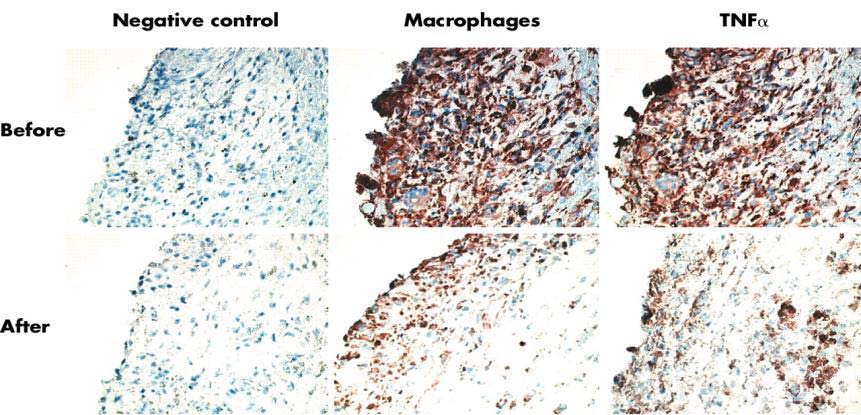
Krootet al.Annals of the Rheumatic Diseases2005
GCTTS的治疗
3中心系统性回顾分析最大
294名GCTTS患者(254例初诊+40首次复发,排除手、足L-GCTTS)
分布:69%D-GCTTS,31%L-GCTTS
结局:局部失败(localfailure,LF)--局部复发+局部进展,5年局部无失败率(5-year-LFFS)
PalmeriniE. et al., EurJ Cancer (2014)
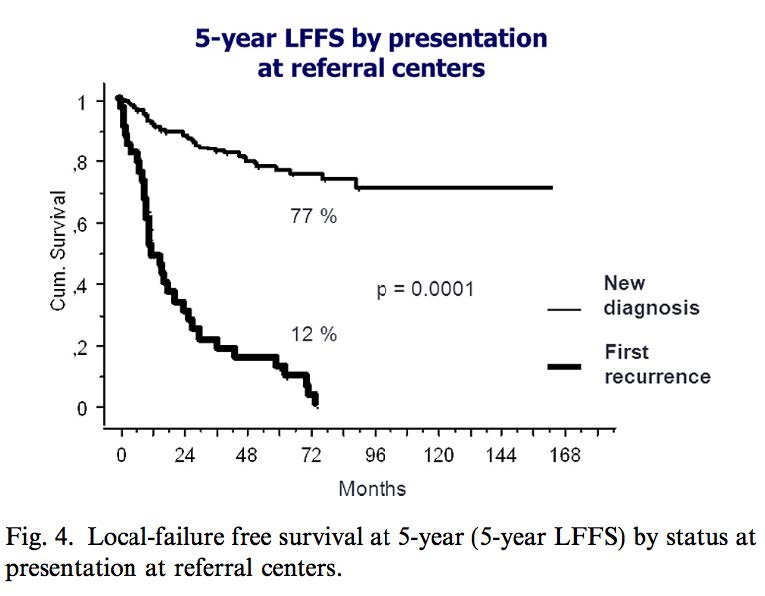
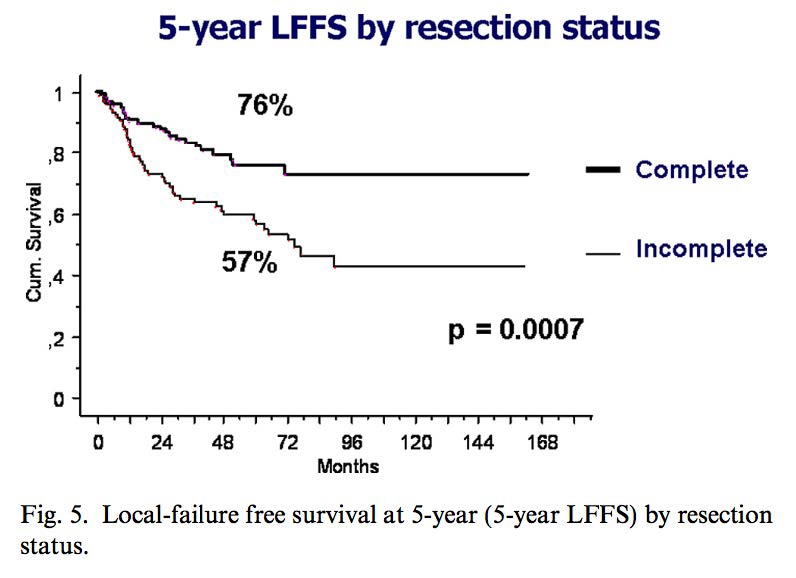
GCTTS的治疗
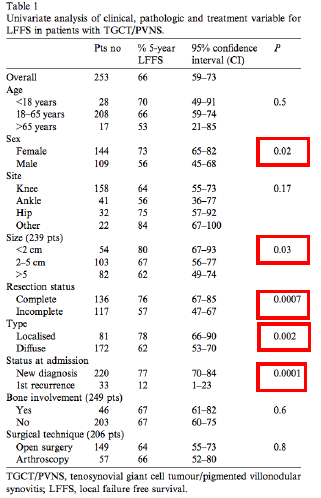
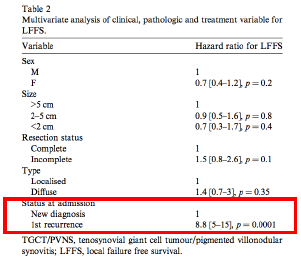

PalmeriniE. et al., EurJ Cancer (2014)
靶向治疗能否“出奇制胜”?
染色体异常

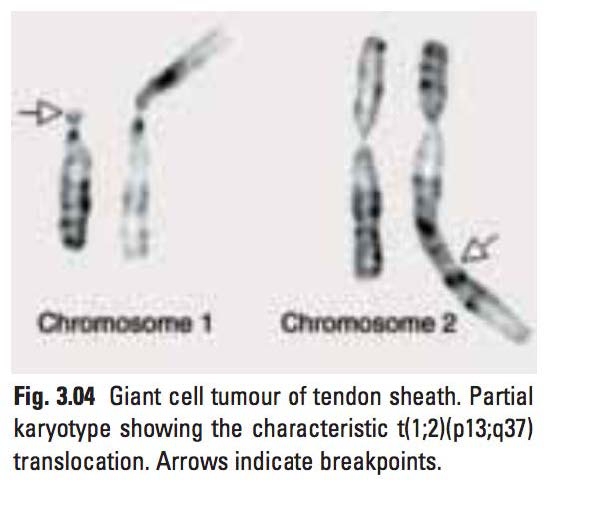
SciotR,ModPathol. 1999 Jun;12(6):576-9. Nilsson,VirchowsArch (2002) 441:475–480
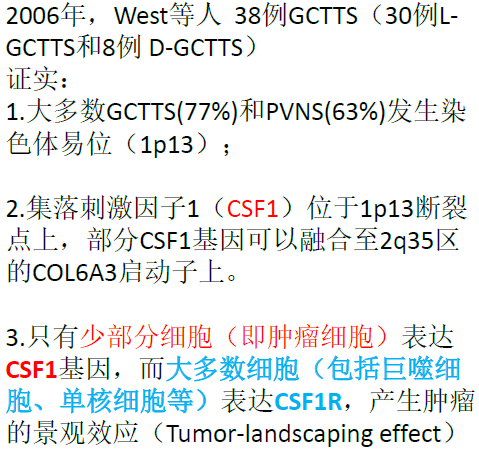
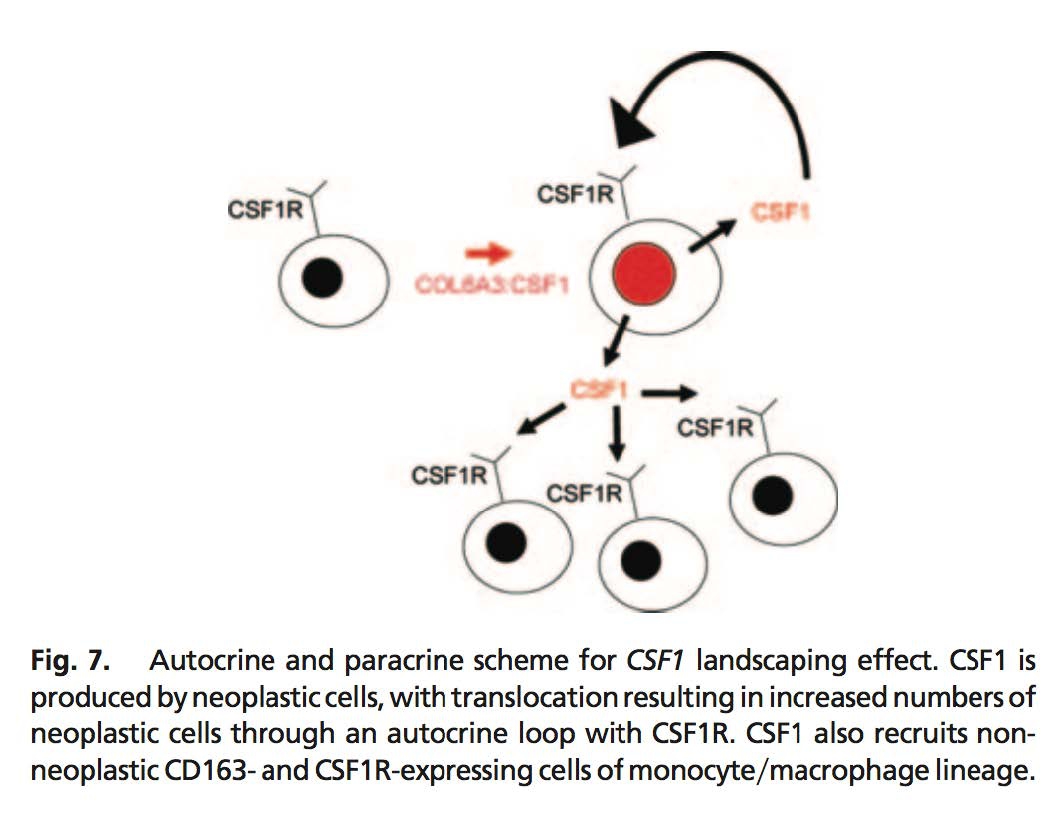
Robert B. West ,ProcNatlAcadSciU S A. 2006 Jan 17;103(3):690-5.

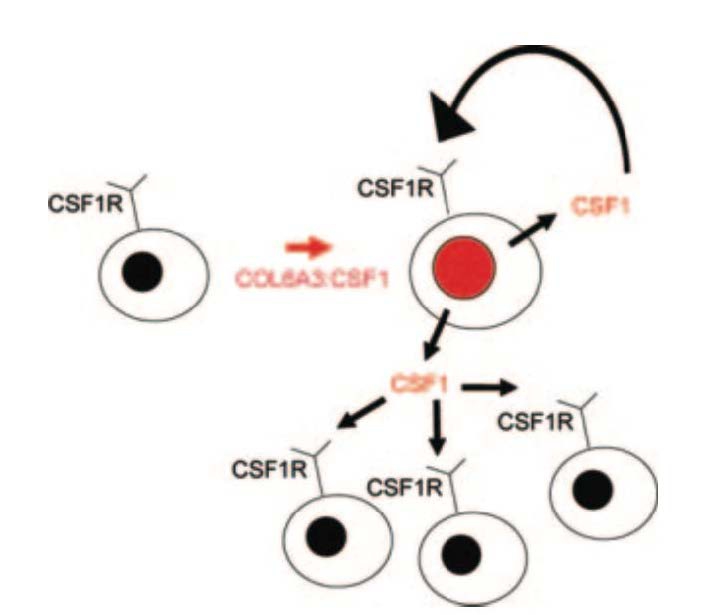
靶向治疗——CSF-1R
CSF-1R单克隆抗体——RG7155(emactuzumab)
临床前研究
7例advanced D-GCTTS
RG7155i.v.biw
第4周评估
5(71%)/7PR(部分缓解)(RECIST评分)
7(100%)/7 PMR(其中2例CMR)
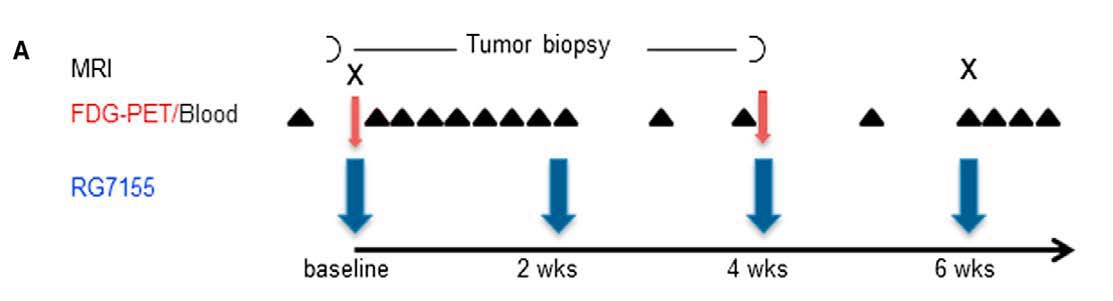

Rieset al., Targeting Tumor-Associated Macrophages with Anti-CSF-1R Antibody Reveals a Strategy for Cancer Therapy, Cancer Cell (2014)
靶向治疗——CSF-1R RG7155(emactuzumab)
女性,19yr
右踝Dt-GCT复发
MR & PET-CT(SUVmax值)
免疫组化:CD68+、CSF-1R
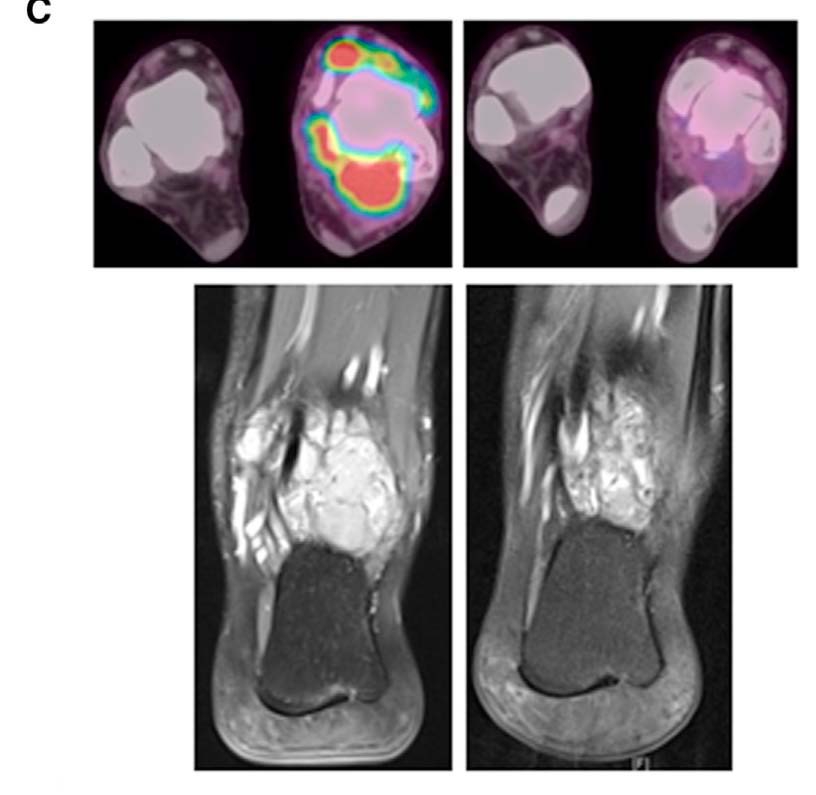
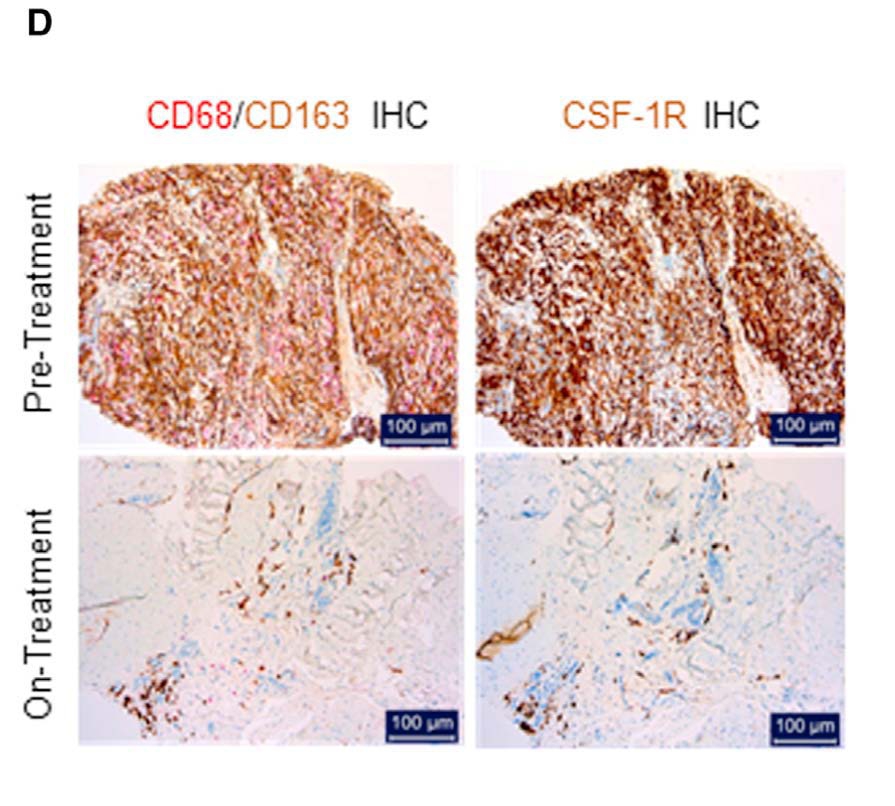
Rieset al., Targeting Tumor-Associated Macrophages with Anti-CSF-1R Antibody Reveals a Strategy for Cancer Therapy, Cancer Cell (2014)
靶向治疗——CSF-1R RG7155(emactuzumab)
I期临床试验:多中心、非盲
剂量递增(dose-escalation)试验:12例
最佳剂量:1000mg i.v.biw
剂量延伸(dose-expansion)试验:17例
常见不良反应:面部水肿(64%)、无力(56%)、皮肤搔痒(56%)

CSF1R inhibition with emactuzumabin locally advanced diffuse-type tenosynovialgiant cell tumoursof the soft tissue: a dose-escalation and dose-expansion phase 1 study ,Lancet Oncol2015;16:949-56
靶向治疗——CSF-1R
24(86%)/28objective response(客观缓解)
2(7%)CR 22(79%)PR
24(92%)/26metabolic response
1(4%)CR 23(88%)PR
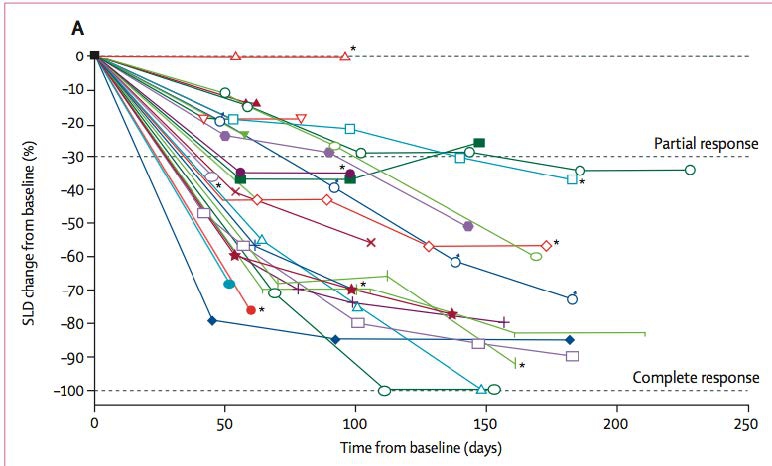
CSF1R inhibition with emactuzumabin locally advanced diffuse-type tenosynovialgiant cell tumoursof the soft tissue: a dose-escalation and dose-expansion phase 1 study ,Lancet Oncol2015;16:949-56
靶向治疗——CSF-1R
选择性CSF-1R抑制剂——PLX3397
I期及II期临床试验:
剂量递增(dose-escalation)阶段:41例
最佳剂量:1000mg p.o.qd
剂量延伸(dose-expansion)阶段:23例
常见不良反应:头发颜色改变、恶心、味觉改变、眼周水肿
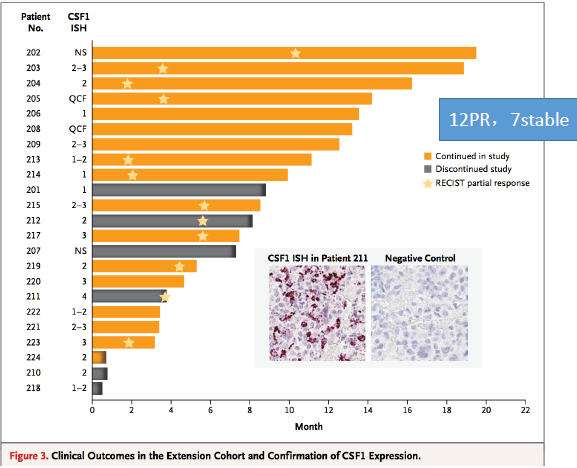
Structure-Guided Blockade of CSF1R Kinase in TenosynovialGiant-Cell Tumor ,The New England Journal of Medicine ,2015,373;5
靶向治疗——CSF-1R PLX3397
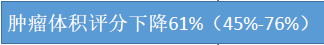
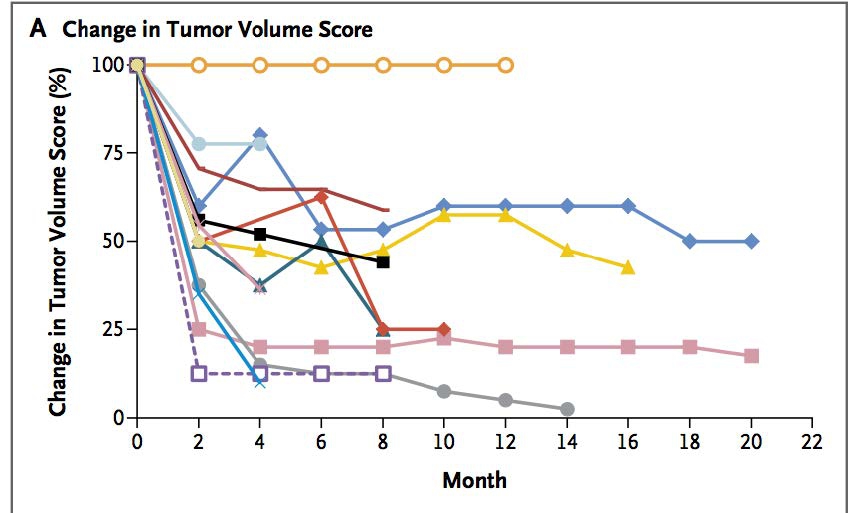

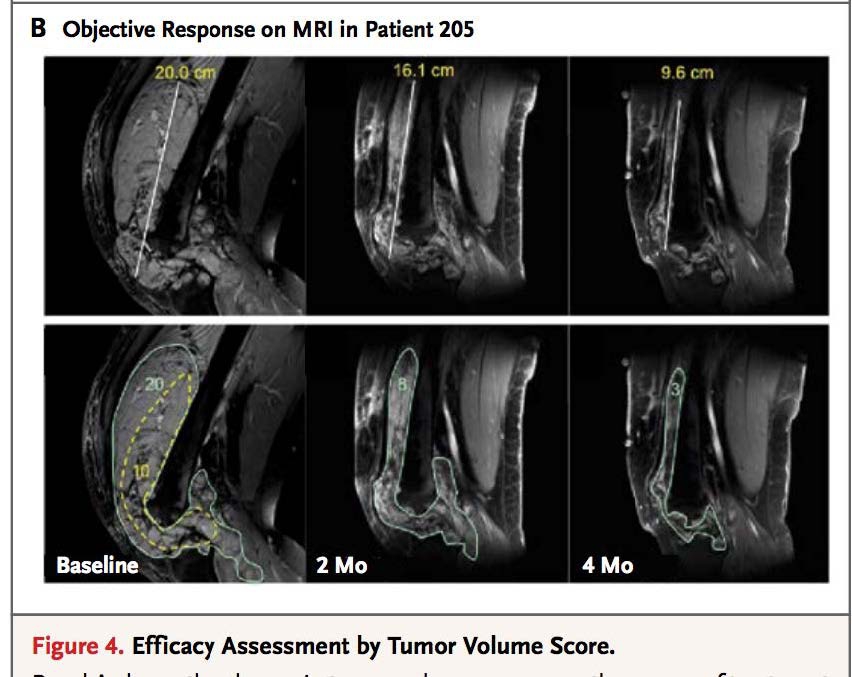
14(100%)/14objective response(客观缓解)
其中,11PR 3stable
Structure-Guided Blockade of CSF1R Kinase in TenosynovialGiant-Cell Tumor ,The New England Journal of Medicine ,2015,373;5
总结
1.腱鞘巨细胞瘤(GCTTS)是良性增殖性肿瘤,弥漫性巨细胞瘤(D-GCTTS)和腱鞘巨细胞瘤局限型(L-GCTTS)基因学和组织学同源,临床表现截然不同。
2.D-GCTTS的诊断需结合临床+影像学+组织学三方面的证据,确诊依靠组织学。
3.D-GCTTS治疗首选仍为手术治疗,并根据发病部位、疾病特点、病人意愿等进行个体化治疗。
4.靶向治疗(CSF-1/CSF1R轴)可能是治疗D-GCTTS的“奇兵”,在未来的治疗方案选择中扮演重要的角色。


 京公网安备11010502051256号
京公网安备11010502051256号